
Głównym celem badań klinicznych jest jak najdokładniejsze przedstawienie rzeczywistych wyników, a projekt badania ma duży wpływ na to, czy przyjąć lub odrzucić wstępną hipotezę. Źle zaprojektowane badanie może przynieść fałszywe wyniki przy ogromnym nakładzie czasu i pieniędzy. Z drugiej strony solidne dane, wygenerowane z dobrze zaprojektowanego projektu można analizować na wiele sposobów, aby uzyskać cenne informacje. W związku z tym odpowiedni projekt ma kluczowe znaczenie dla badania klinicznego. Więc jakie są kluczowe parametry dla metodologii badania?
Cel badania
Założenie badania jest fundamentem, wokół którego opracowywany jest projekt, a dobrze zdefiniowany cel badawczy jest niezbędny do sformułowania hipotezy, którą można przetestować w trakcie badania, niezależnie od tego, czy ma na celu udowodnienie przewagi badanej terapii nad placebo, czy zakłada porównanie do istniejącego standardu opieki medycznej lub równoważność leku generycznego.
Po opisaniu celu badania łatwiej jest określić rodzaj badania, które można przeprowadzić. Najogólniej badania kliniczne można podzielić na interwencyjne lub obserwacyjne. Jak sama nazwa wskazuje, badania interwencyjne przeprowadzane są w celu zbadania efektu nowego leczenia, zwykle metodą pojedynczo lub podwójnie ślepej próby, często w porównaniu z placebo lub kontrolą standardową i obejmują badania kliniczne fazy 1-3 , szczegółowo opisane w poprzednim artykule. Z drugiej strony badania obserwacyjne, badania fazy 4, badania kohortowe oraz badania przekrojowe dotyczą takich kwestii, jak rzeczywiste działanie zatwierdzonych produktów leczniczych, identyfikacja rzadko występujących działań niepożądanych lub rejestrowanie danych dotyczących określonych populacji pacjentów. Ogólnie rzecz biorąc, większość przeprowadzonych badań klinicznych ma charakter interwencyjny[1] . Jednak badania obserwacyjne również odgrywają istotną rolę w gromadzeniu danych pochodzących z codziennie praktyki (real world data), identyfikowaniu metod klinicznych i markerów zdrowia. W hierarchii dowodowej randomizowane badania kontrolne (Randomized Controlled Trials, RCT) zajmują jeden z najwyższych poziomów, poprzedzone jedynie przeglądami systematycznymi RCT (metaanalizami) (ryc. 1).
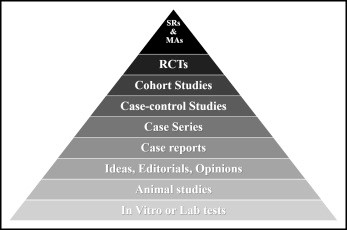
Grupa pacjentów
Identyfikacja populacji docelowej ma ogromne znaczenie dla projektu badania. Parametry takie jak wskazanie, w którym prowadzone ma być badanie, płeć, wiek, pochodzenie etniczne, styl życia, itd. muszą zostać określone z góry, aby zidentyfikować kryteria kwalifikujące pacjenta do włączenia do badania. W związku z tym dobrze zdefiniowana lista kryteriów włączenia pomaga w skutecznej rekrutacji uczestników badania. Zasięgniecie opinii klinicystów – ekspertów w badanej dziedzinie terapeutycznej może być bardzo cenne, a w niektórych przypadkach może znacznie przyspieszyć proces. W ramach przygotowywanie jednego z naszych projektów omówiliśmy proponowane kryteria kwalifikacyjne do badania klinicznego z potencjalnym badaczem co pozwoliło ustalić, że pacjenci, którzy zostaliby wykluczeni, z klinicznego punktu widzenia mogą kwalifikować się do badania, a zmiana nie ma negatywnego wpływu na wyniki. Nasze ustalenia pomogły sponsorowi zrewidować założenia protokołu i dzięki temu osiągnąć wyższą i szybszą rekrutację, tym samym skracając czas trwania badania.
Procedury badania
Określenie koniecznych do przeprowadzenia procedur badania jest kolejnym ważnym aspektem projektu badania, ponieważ odpowiednie metody oceny poszczególnych parametrów będą decydować o jakości i wartości analitycznej danych zebranych w trakcie badania. Istotne jest więc zaoferowanie zespołowi projektującemu badanie wsparcia w optymalizacji procedur badawczych w celu pozyskania wysokiej jakości danych.
Analiza statystyczna
Wiarygodność wyników badania zależy w ogromniej mierze od wartości i jakości analizy statystycznej. Przed rozpoczęciem badania opracowywany jest Plan analizy statystycznej w celu obiektywnej oceny wyników badania. Wielkość próby musi być wystarczająco duża, aby zidentyfikować rzeczywiste i istotne statystycznie różnice między badanymi grupami. Zbyt mała próbka zmniejsza moc badania, podczas gdy zbyt duża liczba wpływa na bardziej praktyczne aspekty projektu, takie jak czas trwania badania, obciążenie finansowe i zaangażowanie personelu, itp. Identyfikacja oczekiwanych wyników badania pomaga w oszacowaniu, jaka zmiana będzie znamienna statystycznie. Na przykład obniżenie ciśnienia krwi po podaniu nowego leku przeciwnadciśnieniowego lub zmniejszenie wartości glikowanej hemoglobiny u pacjentów z cukrzycą po terapii nową insuliną.
Praktyczne aspekty badania
Po przeprowadzeniu powyższych etapów w proces projektowania badania powinniśmy skoncentrować się na bardziej praktycznych aspektach. Pytania takie jak czas trwania badania, liczba ośrodków potrzebnych do zapewnienia rekrutacji uczestników, wyposażenie i infrastruktura ośrodków itp. mają również znaczenie i należy się nimi zająć przy projektowaniu badania. Istotne dla tego etapu są uwarunkowania krajowe, regionalne i lokalne. Materiały dla pacjentów, takie jak formularz świadomej zgody, ulotka informacyjna, kwestionariusze, dzienniczki itp. muszą być przygotowane nie tylko w języku angielskim, ale także w językach lokalnych. Biorąc pod uwagę różne wymagania w różnych krajach europejskich, pomagamy naszym klientom w przygotowaniu specjalistycznych materiałów, uwzględniając miejsce prowadzenia planowanego badania klinicznego.
Podsumowując, odpowiednie zaprojektowanie badania jest podstawą, która pozwoli przeprowadzić projekt w taki sposób, aby pierwotną hipotezę badawczą przełożyć na sensowne wnioski, a w konsekwencji osiągnąć zamierzony cel.
Autor: Krystyna Iwińska, ACT
www.actrials.com
krystyna.iwinska@actrials.com
Profil LinkedIn
Źródła:
[1] https://clinicaltrials.gov/ct2/resources/trends
[2] Sackett DL. Rules of evidence and clinical recommendations on the use of antithrombotic agents. Chest. 1989;95(2Suppl):2S-4S.




